PPS 點擊 藍字關注我們↑↑↑↑ 專家介紹:徐寒梅 中國藥科大學生命科學與技術學院教授,博士生導師,海洋藥學教研室主任,江蘇省合成多肽藥物發現與評價研究工程中心主任。近 5 年以來,先后主持:國家自然科學基金,國家“863”高科技發展計劃,國家“十一
專家介紹:徐寒梅

中國藥科大學生命科學與技術學院教授,博士生導師,海洋藥學教研室主任,江蘇省合成多肽藥物發現與評價研究工程中心主任。近 5 年以來,先后主持:國家自然科學基金,國家“863”高科技發展計劃,國家“十一五”、“十二五”、“重大新藥創制”科技重大專項,江蘇省校企合作前瞻性研究等項目,近 5 年帶領課題組(包括南京大學、武漢大學、廣州藥學院、醫藥企業)獲得國家資助 3 800 余萬元,并帶領團隊成功申報多個 1 類新藥臨床批件。因與企業合作抗腫瘤多肽研究的表現獲得內蒙古自治區“杰出創新引進人才”獎,“草原英才”,近 5 年先后獲得江蘇省“青藍工程”優秀骨干教師,中青年學術帶頭人,南京市領軍人才等獎勵和稱號,因為產學研合作的表現被內蒙古自治區政府聘為科技特派員,被教育部“藍火工程”聘為泰州市科技特派員。
正文
CD47 相關信號通路及其與相關疾病關系的研究進展
葛闖 , 胡加亮 , 徐寒梅 *
(中國藥科大學 江蘇省合成多肽藥物發現與評價工程研究中心,江蘇 南京 211198)
[摘要]CD47 是一種在細胞表面普遍表達的糖蛋白,能與多種胞內外蛋白如凝血栓蛋白 1(TSP1)和信號調節蛋白 α(SIRPα)發生相互作用,參與多種信號通路的調控,這些信號通路在多種疾病如腫瘤、心血管疾病和自身免疫性疾病的發生和發展過程中起著重要的作用。通過重點闡述 CD47 的結構、表達、與其他蛋白的相互作用、相關的信號通路以及其與疾病的關系,以期為靶向 CD47 的治療策略的開發提供幫助。
整合素相關蛋白 CD47 最初發現于無 Rh 抗原性溶血性貧血患者體內,其血紅細胞缺乏CD47。前期研究發現,CD47 與整合素 αvβ3,αⅡbβ3 和 α2β1 相互作用,調節整合素功能和調節細胞對含有精氨酸-甘氨酸-天冬氨酸的胞外基質蛋白的應答,因而被稱作整合素相關蛋白。CD47 在多種腫瘤中表達升高,如卵巢癌、白血病、乳腺癌、結腸癌、膀胱癌、膠質母細胞瘤、肝細胞癌和前列腺腫瘤等。研究表明,抗 CD47 抗體能夠刺激巨噬細胞清除腫瘤細胞,因而 CD47 成為近年來研究的熱點。
CD47 通過與胞外、胞內以及其他的跨膜蛋白的橫向相互作用發揮不同的功能,介導了不同的信號轉導通路,這些信號通路在腫瘤、血管類疾病、自體免疫性疾病等多種疾病中發揮著不同作用。
1CD47 結構、表達與相互作用
1.1 結構
CD47 屬于免疫球蛋白超家族,有 2 種異構體,一種含有 N 糖基化修飾,另一種在其 64 位和 79 位絲氨酸含有糖胺聚糖修飾。CD47 結構包含 3 個部分,N 末端胞外免疫球蛋白多變(IgV)結構域、高度疏水的 5 次跨膜片段和 1 個短的多變 C 末端胞內段,如圖 1 所示。
CD47 通過胞外段 IgV 結構域與其配體凝血栓蛋白 1(thrombospondin 1,TSP1)和信號調節蛋白 α(signal regulatory protein alpha,SIRPα)相互作用,IgV 結構域被 N 糖基化和 O-連接型糖胺聚糖修飾,糖胺聚糖修飾是 CD47 與 TSP 相互作用所必需的。IgV 結構域上的氨基酸殘基 Cys33 與跨膜區最后一個胞外環上的氨基酸殘基 Cys263 之間存在長二硫鍵,這一二硫鍵對于 CD47 配體的結合、信號轉導以及定位到脂筏都是必要的。胞內段存在 4 種可變剪接體形式,根據基因結構、多肽序列不同,分為Ⅰ型、Ⅱ型、Ⅲ型和Ⅳ型,氨基酸數量從 3~36 個不等。Ⅱ型是目前最主要的、表達最多的異構體,其次是Ⅳ型,Ⅳ型主要在腦部和外周神經系統表達,而 I 型只在角質細胞中顯著表達,Ⅲ型主要與記憶鞏固相關。

1.2 表達
CD47 在幾乎所有的細胞表面都有表達,包括紅細胞和血小板,其表達水平因機體的免疫狀態或病理狀態不同而改變。CD47在多種腫瘤中表達較高,并且通過阻斷CD47 能夠增強腫瘤的吞噬作用。Xu 等發現抗 CD47 治療可增加巨噬細胞的吞噬功能,降低腫瘤重量,并抑制骨肉瘤異種移植模型中的自發轉移。Zhang 等發現阻斷 CD47 可增強巨噬細胞對腫瘤細胞的吞噬作用,減輕腫瘤負荷,提高膠質母細胞瘤患者的存活率。同樣地,Yoshida等也發現通過阻斷 CD47 能增強巨噬細胞對胃癌細胞的吞噬作用。以上均表明 CD47 可能是腫瘤細胞的一個重要生存信號分子,與腫瘤發生發展密切相關。在免疫應答過程中,CD47 在 CD4 效應 T 細胞表面表達升高,防止記憶性 T 細胞被巨噬細胞清除,延長生存周期。同樣,造血干細胞(hematopoietic stem cells,HSCs)表面 CD47 高表達也使其免受巨噬細胞吞噬,而當 CD47 在 CD34+ CD38-HSCs 表面表達選擇性下調時,就有可能發生噬血細胞綜合征(hemophagocytic lymphohistiocytosis,HLH)。
1.3相互作用
CD47 通過胞外 IgV 結構域主要與 3 種胞外配體相互作用,分別為 CD47-TSP1、CD47-SIRPα 及CD47-CD47。由于 CD47 胞內結構域較小,只有有限的幾種胞內信號蛋白與 CD47 相互作用,主要是促凋亡調節蛋白(BCL2/adenovirus E1B 19 kDaprotein-interacting protein 3,BNIP3)以及連接整合素相關蛋白和細胞骨架蛋白(protein-linking integrinassociated protein and cytoskeleton,PLIC)。而 CD47 與其他跨膜蛋白的橫向相互作用可能在CD47 的信號轉導通路中發揮著重要作用,如整合素 αvβ3、血管內皮細胞生長因子受體 2(vascular endothelial growth factor receptor 2,VEGFR2)、Rh血型抗原肽復合物、CD47、自殺相關因子(factor associated suicide,Fas)、CD14 等。
1.3.1 胞外相互作用 首先被發現的 CD47 內源性配體就是 TSP1。TSP1 屬于 TSP 家族成員之一,這一家族除了 TSP1 之外,還包括 TSP2 ~TSP5。TSP1是一種瞬時表達的細胞基質蛋白,在不同環境中,通過與細胞表面受體或其他的胞外基質成分相結合調節細胞功能。TSP1 結構很大,包含多種結構域,使其能與多種細胞表面受體和胞外基質相互作用,包括整合素(主要是 β1 和 β3)、CD47、CD36、硫酸乙酰肝素蛋白多糖、低密度脂蛋白相關蛋白 1 和極低密度脂蛋白受體等。TSP1 通過其碳末端結合 結 構 域(C-terminal binding domain)上的 VVM 序列與 CD47 相結合,進而影響多種細胞功能,如細胞遷移和黏附、細胞增殖和凋亡、調節血管生成和炎癥反應等。
第 2 個被發現的內源性配體是 SIRPα。SIRPα屬于免疫球蛋白超家族,是一種跨膜蛋白,表達在骨髓細胞表面,如單核細胞、巨噬細胞、粒細胞和CD4 陽性樹突狀細胞,以及在中樞神經系統神經元細胞中以不同水平表達。SIRPα 在吞噬細胞表面表達水平似乎非常穩定,不會受到炎癥水平的影響,而 CD47 的表達卻隨不同的免疫狀態或疾病的改變而改變。SIRPα 胞外 N 末端包含 3 個 Ig 樣結構域,1 個單一的跨膜結構域,胞漿 C 末端含有 4 個酪氨酸殘基,帶有 2 個免疫受體酪氨酸抑制基序(immunoreceptor tyrosine-based inhibitory motif,ITIM),ITIM 是酪氨酸磷酸酶 SHP(src-homology domain 2-containing protein tyrosine phosphatase)-1和 SHP-2 的結合位點,ITIM 介導 SHP-1 和 SHP-2 的募集和激活,使得磷酸化蛋白底物去磷酸化,從而影響胞內信號通路轉導,如抑制生長因子受體和其他的一些促酪氨酸激酶活性受體的信號轉導。SIRPα 通過其 N 末端 IgV 結構域與 CD47 的 IgV 結構域結合,SIRPα 與 CD47 之間的相互作用在控制細胞吞噬中發揮作用,能夠產生一種“不要吃我”的信號。
除了與 TSP1 和 SIRPα 結合,也有研究表明,細胞間發生黏附需要 CD47 的存在而并不需要其配體,表明 2 個細胞上 CD47 的 IgV 結構域也存在著同型結合。不過這種 CD47 與 CD47 相互作用能否產生信號轉導還缺乏足夠的證據。
1.3.2 膜表面相互作用 CD47 首先被發現與整合素 αvβ3 存在相互作用,后續又發現其與多種整合素亞型相互作用,如 αⅡbβ3、α2β1、αLβ2、和 α4β1。CD47 通過其 IgV 結構域與整合素 αvβ3 發生相互作用,激活整合素,從而引發后續的胞內信號轉導,而并不依賴其跨膜結構域。CD47 與這些整合素發生結合,相互作用,能夠改變整合素信號靶點,如黏著斑激酶和樁蛋白,并且 CD47-整合素復合體還與三聚體 G 蛋白相關,參與調控 cAMP 信號轉導。
CD47 能夠與血管內皮細胞生長因子(vascular endothelial growth factor,VEGF)以及 VEGFR2 發生相互作用。而 TSP1 能夠通過 CD47 抑制 VEGF 下游信號級聯通路。此外,免疫共沉淀和熒光共振能量轉移表明,CD47 能夠與 VEGFR2 直接發生相互作用,不過這種相互作用會因 TSP1 和 CD47 結合以及VEGF 與 VEGFR2 結合而被破壞,從而抑制 VEGFR2信號轉導過程。
在紅細胞中,CD47 與 Rh 抗原復合體相互作用,形成復合體,這一復合體通過錨定蛋白與細胞骨架上的血影蛋白連接,有助于維持紅細胞形態和氨的運輸,不過 CD47 在其中的功能尚不清楚。
在 T 細胞中,Fas 被發現與 CD47 發生橫向相互作用。只有在表達 CD47 的細胞中,通過激活 Fas 才能夠引起細胞凋亡。CD47 與 Fas 的相互作用對于 Fas 下游的信號通路包括 caspase-7 和聚腺苷酸二磷酸 核糖轉移酶(poly ADP-ribose polymerase,PARP)裂解都是必要的。
1.3.3 胞內相互作用 將 CD47 跨膜結構域和 C 末端尾巴作為酵母雙雜交系統誘餌,從人類淋巴細胞cDNA文庫中篩選,發現BNIP3是其胞漿結合配體。反向抑制 BNIP3 能夠抑制 CD47 介導的細胞凋亡,而用TSP1激活CD47能夠誘導BNIP3轉移到線粒體,導致細胞死亡,而 SIRPα 與 CD47 結合并不能引起 BNIP3 轉移。
利用 CD47 胞漿尾巴的整合素相關蛋白-2(integrin associated protein-2,IAP2) 和 IAP4 剪切異構體作為酵母雙雜交系統誘餌鑒別出了另外2 種泛素相關蛋白作為 CD47 胞漿結合配體,分別是連接整合素相關蛋白和細胞骨架蛋白 PLIC1 和 PLIC2,后續研究發現 PLIC1 結合 G 蛋白 βγ 亞基(Gβγ),從而使 CD47 與三聚體 G 蛋白相結合,調節其下游信號通路。
2CD47 相關信號通路
在胞外與 CD47 相互作用的配體分別是 TSP1、SIRPα 和 CD47 自身。其中,目前對 CD47 自身的同型相互作用參與的信號轉導知之甚少。因此,目前 CD47 主要參與的信號通路可以按胞外與之相互作用的配體大致分為 2 個方面,即 TSP1 和 SIRPα分別與 CD47 相互作用參與調控的信號通路,如圖2 所示。
2.1 CD47/TSP-1 相關通路
2.1.1 調控 G 蛋白通路 CD47 與整合素形成的復合體可通過其胞內配體 PLIC1 與三聚體 G 蛋白相互作用,形成 CD47-整合素-G 蛋白復合體。CD47 的5 個跨膜結構域與其配體整合素的 2 個 TM 片段形成一個臨時的 7 次跨膜復合體(7TMS),7TMS 能夠激活 G 蛋白。不同的整合素配體以及具有不同胞漿尾巴的 CD47 異構體都能夠使 7TMS 復合體具有激活特異性三聚體 G 蛋白的功能。G 蛋白可以介導 CD47 多種細胞效應,如 CD47 相關的血小板激活需要 G 蛋白激活 Syk 激酶,從而誘導 Lyn 和 FAK 磷酸化。CD47-整合素-G 蛋白復合體的另一成分是膽固醇。去除膽固醇不會影響整合素親和性,但會降低 CD47 刺激細胞黏附到玻連蛋白的能力。因此,雖然細胞基本的擴散機制與膽固醇無關,但是膽固醇似乎對保持功能性的 CD47-整合素-G 蛋白復合體起著必要的作用。

2.1.2 調控 NO/cGMP 信號通路 在血管細胞中,內皮一氧化氮合酶(endothelial NO synthase,eNOs)是主要的一氧化氮(NO)合酶異構體,它能將 L精氨酸轉變成 L-瓜氨酸并釋放 NO。eNOs 活性受到機械刺激和循環因子如 VEGF 和乙酰膽堿的調控。VEGF 通過內皮細胞上的 VEGFR2 激活 PI3K,后者激活蛋白激酶 B(protein kinase B,PKB,又稱為 Akt),Akt 磷酸化 eNOs 上的第 1177 位絲氨酸,使其激活。同時活化的 VEGFR2 募集 Src 并誘導Ca2+ 信號通路,進一步激活 eNOs。產生的 NO 結合靶細胞中可溶性鳥苷酸環化酶(soluble guanylatecyclase,sGC)的血紅素結構,增加其酶催化活性,導致胞內 cGMP 積聚,cGMP 激活 cGMP 依賴性激酶 1(cGMP-dependent protein kinase,cGK1), 后者磷酸化肌球蛋白輕鏈激酶并抑制其活性,使得肌球蛋白輕鏈脫磷酸化而引起平滑肌松弛。TSP1能夠與 CD47 結合,破壞 CD47 與 VEGFR2 復合體,抑制 VEGFR2 激活,進而影響下游信號通路。
2.1.3 調控細胞生存 TSP1 與 CD47 結合能夠誘導BNIP3 轉移到線粒體,BNIP3 跨膜結構域插入到線粒體膜,引起線粒體通透性轉換孔打開,釋放細胞色素 C,導致細胞死亡。缺乏 CD47 有助于細胞通過激活保護性的自噬通路促進其生存。自噬是一種維持內環境穩定的分解代謝機制,是胞質溶膠和細胞器被隔離到雙層膜的小泡中,由此運送到溶酶體/空泡中降解,并因此形成的大分子進行再循環的一個過程。輕度的自噬可以防止細胞被不利因素損害,有助于其生存。缺乏 CD47 的細胞受到輻射時,beclin-1、ATG5、 ATG7 表達升高,p62 表達降低,LC3 表達升高,自噬小體形成增多,激活保護性自噬。其中 Beclin-1 也能夠與 Bcl-2/Bcl-xL 結合構成復合體,從而自噬的激活過程將會受到抑制,因此,Beclin-1與Bcl-2相互作用可直接控制自噬與凋亡。
2.2CD47/SIRPα 相關通路
2.2.1 調控吞噬作用 CD47 作為一種自體的識別分子,或者是作為一種“不要吃我”的信號分子,能夠與巨噬細胞表面的 SIRPα 相互作用,防止腫瘤細胞和紅細胞被清除。這種防止巨噬細胞吞噬的機制涉及到 SIRPα 的抑制性信號通路,其中部分是通過 SHP-1 來抑制巨噬細胞吞噬作用。
此外,有研究發現,CD47-SIRPα 相互作用在紅細胞清除方面的功能可能要更為復雜。人體紅細胞的衰老似乎與 CD47 的構象改變有關,可能是依賴于氧化修飾,其能夠將分子從“不要吃我”轉變為“吃我”的結構。因此,CD47 不僅是一種“不要吃我”的信號,也可能是作為一種調節紅細胞清除的開關。因此,CD47 或者 SIRPα 表達異常或相互作用受到干擾都會改變巨噬細胞的吞噬作用,破壞紅細胞的體內穩態。
2.2.2 調節樹突狀細胞和 T 細胞體內穩態 有研究發現,SIRPα 變異小鼠的脾臟 CD4+DC 細胞數量減少,半衰期降低,脾臟中 CD4+T 細胞數量減少,T 細胞聚集區域變小 。表明 CD47 與 SIRPα 相互作用對于調節樹突狀(DC)細胞和 T 細胞體內穩態具有重要的作用。此外有研究發現,DC 細胞和 T 細胞應答在多種水平上受到 CD47 與 SIRPα 相互作用的影響,CD47 與 SIRPα 相互作用受到干擾會使得 DC細胞功能受損,尤其是在誘導輔助性 T 細胞 Th1、Th2、Th17 和自然殺傷性 T 細 胞(natural killer Tcell,NKT)應答方面 。
3CD47 相關信號通路與疾病的關系
3.1 癌癥
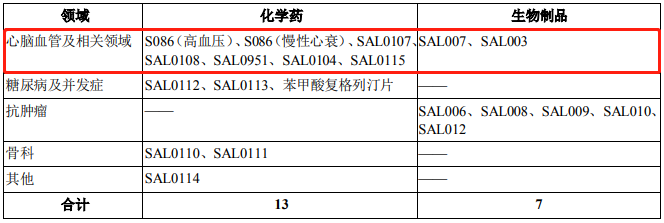
CD47 在多種腫瘤細胞表面高表達,其作為一種“不要吃我”的信號分子,與巨噬細胞表面SIRPα相互作用,從而使腫瘤細胞避免被吞噬清除,增強腫瘤生存能力。因此,靶向 CD47-SIRPα相互作用可能成為腫瘤治療的一種新策略。目前抗腫瘤治療主要靶向 CD47-SIRPα 軸,多種治療藥物已處于臨床研究階段,包括常規抗體,融合蛋白和雙特異性分子,分別阻斷 CD47 或SIRPα(見表 1)。

3.2 心血管疾病
心血管疾病主要的臨床表現包括卒中、黃斑變性、外周血管病、高血壓、心臟和其他關鍵器官衰竭、心臟病、傷口愈合不良等。其病因主要是急性或亞急性血流量下降并伴隨組織低灌注,而血管細胞內 NO 信號通路受損是導致心血管疾病的關鍵因素。在衰老過程中,內源性 NO 合成減少而 TSP1表達升高。如前所述,TSP1 和 CD47 相互作用能夠抑制 NO/cGMP 信號通路,因此抑制 TSP1-CD47 相互作用能夠改善 NO 信號通路,減輕心血管疾病的發生。
Kojima 等采用 CD47 阻斷抗體 MIAP410,發現體外可誘導病變的、死亡的與即將死亡的平滑肌細胞和巨噬細胞被清除,并在幾種不同的動脈粥樣硬化小鼠中,利用抗 CD47 抗體阻斷 CD47,從而顯著地阻止動脈斑塊堆積,使病變血管組織的清除恢復正常。
3.3自身免疫性疾病
有研究表明,SIRPα 和 CD47 與 Th1 細胞或Th17 細胞相關的自身免疫性疾病的形成有關,如實驗性變態反應性腦脊髓炎(experimental autoimmuneencephalomyelitis,EAE)、細菌或膠原誘導的關節炎、接觸性超敏反應、結腸炎、克羅恩病等。如前所述,CD47-SIRPα 相互作用對 DC 細胞的功能具有調節作用,尤其是遷移和抗原呈遞,其對于激活自身反應性 Th1 細胞和 Th17 細胞是必須的。在關節炎、結腸炎和克羅恩病中,干擾 CD47-SIRPα 相互作用能夠抑制病情,然而在EAE中卻會加重自身免疫和相關疾病。研究表明,SIRPα缺失小鼠或者給予抗SIRPα抗體(P84)能夠顯著減輕Ⅱ型膠原型關節炎小鼠的炎癥水平、骨侵蝕和關節炎癥狀。
3.4 噬血細胞綜合征
HLH 典型特征之一就是噬血細胞作用增強,主要是由于細胞毒性 T 淋巴細胞(cytotoxic lymphocyte,CTL)和 NK 細胞清除病原功能受損,導致巨噬細胞過度增殖,噬血細胞增多。CD47 在 HLH 的CD34+CD38-HSCs 中表達下調,巨噬細胞對其吞噬作用增強,從而發生噬血細胞綜合征。
4 結語與展望
CD47 與其 2 個配體 TSP1 和 SIRPα 相互作用,參與多種信號通路,參與機體多種生理功能及病理過程的發生發展,因此靶向 CD47 為疾病的治療提供了一種新的方法。目前,靶向 CD47 的治療主要還是集中在抗腫瘤領域,治療策略主要有阻斷抗體、重組融合蛋白、反義 RNA、小分子抑制劑,其中阻斷抗體和重組融合蛋白研究較多,主要是分別靶向 CD47 及其 2 個配體 SIRPα 和 TSP1。目前國際上處于 I 期臨床的靶向 CD47 的抗腫瘤藥物包括Hu5F9-G4、CC-90002、TTI-621、ALX148 等, 其中 TTI-621 是可溶性重組 SIRPα-Fc 融合蛋白,其穿透能力和組織分布性較好,與紅細胞的親和力也更低,安全性更高。國內走在前列的是宜明昂科生物的 IMM01,目前已獲得臨床試驗受理。小分子抑制劑,如多肽,體內半衰期較短,且容易酶解,難以發揮治療作用,但其可用于設計有效穩定的模擬肽,如 TSP-1 的模擬肽,可用于識別其受體 CD36。反義 RNA 能夠阻斷 CD47 mRNA 翻譯,從而抑制CD47 蛋白表達,也有望成為靶向 CD47 的有效手段。總之,CD47 不僅是目前腫瘤領域研究的熱點,在其他多種疾病中也扮演著重要作用,開發靶向 CD47 藥物有望為疾病的治療提供新的策略。
關于藥學進展
感謝您閱讀《藥學進展》微信平臺原創好文,也歡迎各位讀者轉載、引用。本文選自《藥學進展》2020年第5期。
《藥學進展》雜志是由中國藥科大學和中國藥學會共同主辦、國家教育部主管,月刊,80頁,全彩印刷。刊物以反映藥學科研領域的新方法、新成果、新進展、新趨勢為宗旨,以綜述、評述、行業發展報告為特色,以藥學學科進展、技術進展、新藥研發各環節技術信息為重點,是一本專注于醫藥科技前沿與產業動態的專業媒體。
《藥學進展》注重內容策劃、加強組稿約稿、深度挖掘、分析藥學信息資源、在藥學學科進展、科研思路方法、靶點機制探討、新藥研發報告、臨床用藥分析、國際醫藥前沿等方面初具特色;特別是醫藥信息內容以科學前沿與國家戰略需求相合,更加突出前瞻性、權威性、時效性、新穎性、系統性、實戰性。根據最新統計數據,刊物篇均下載率連續三年蟬聯我國醫藥期刊榜首,復合影響因子0.760,具有較高的影響力
《藥學進展》編委會由國家重大專項化學藥總師陳凱先院士擔任主編,編委新藥研發技術鏈政府監管部門、高校科研院所、制藥企業、臨床醫院、CRO、由金融資本及知識產權相關機構百余位極具影響力的專家組成。
《藥學進展》編輯部官網:www.cpupps.cn;郵箱:yxjz@163.com;電話:025-83271227。歡迎投稿、訂閱!
● 想回顧《藥學進展》編委會主辦和協辦過的精彩活動嗎?請戳這里!
→
→
→
→
→
→
→
→
→
→
點一下你會更好看耶
行業動態|耐信?針劑獲批用于預防重癥患者應激性潰瘍出血行業動態|耐信?針劑獲批用于預防重癥患者應激性潰瘍出血
PPS 點擊 藍字關注我們↑↑↑↑ 2020年7月30日,中國上海——阿斯利康今日宣布,國家藥品監督管理局(NMPA)已正式批準耐信?針劑(注射用艾司奧美拉唑鈉)用于預防重癥患者應激性潰瘍出血。作為原研質子泵抑制劑,注射用艾司奧美拉唑鈉這一新適應證獲批為我國...
https://mp.weixin.qq.com/s?__biz=MzA5MDY3ODExNQ==&mid=2651311444&idx=2&sn=69f8bc02da4b74a6673342652dd6f93b&chksm=8bf49b58bc83124e93e71979602b9f60588f779fa7eb582fdb6b3dade90fc0cdd282170327b8#rd
本文來源:藥學進展 作者:藥學進展 免責聲明:該文章版權歸原作者所有,僅代表作者觀點,轉載目的在于傳遞更多信息,并不代表“醫藥行”認同其觀點和對其真實性負責。如涉及作品內容、版權和其他問題,請在30日內與我們聯系
 客服微v信:
客服微v信:








 京公網安備 11010802031568號
京公網安備 11010802031568號

